Espectros Atômicos
| Site: | Moodle UFSC - Apoio aos Cursos Presenciais |
| Curso: | Design Instrucional em Ambiente Virtual de Aprendizagem |
| Livro: | Espectros Atômicos |
| Impresso por: | Usuário visitante |
| Data: | terça-feira, 3 fev. 2026, 04:53 |
Espectros Atômicos
Desde o século XVII, já se sabia que as substâncias aquecidas emitiam luz com espectro discreto.
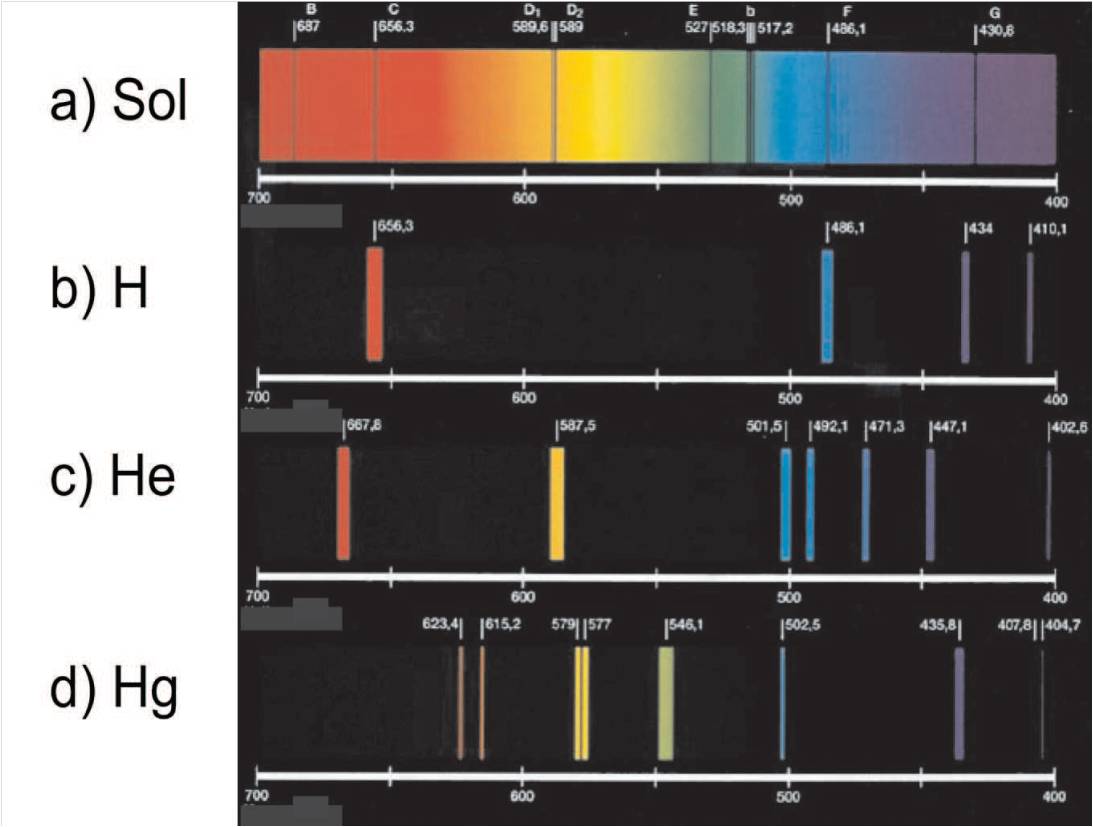
Espectro: conjunto de comprimentos de onda emitidos ou absorvidos pelo elemento.
Espectro de emissão: linhas coloridas obtidas pela dispersão da luz emitida pela amostra. Cada linha corresponde a um determinado comprimento de onda.
Espectro de absorção: linhas escuras obtidas ao transmitir luz branca atraves da amostra. As linhas escuras estão sempre nas mesmas posições das linhas claras emitidas pela mesma amostra. Assim, o espectro de absorção coincide com o espectro de emissão.
As estrelas distantes que podem ser analisadas por meio da medida do espectro. Em colaboração com seu colega químico Robert Bunsen, Kirchhoff transformou a Espectroscopia numa poderosa ferramenta para a análise química de amostras diversas em laboratório. O objetivo, nessa área, e identificar os elementos químicos presentes numa determinada amostra.
Carga Elétrica
Experimento de Milikan
Robert Andrews Millikan (1868-1953) recebeu o prêmio Nobel de Física de 1923 por seus estudos da carga elétrica elementar da eletricidade e do efeito fotoelétrico.
Assista aos vídeos:
moodle.ufsc.br/file.php/17624/millikan/os_curiosos_millikan.flv
e
E procure refletir se as seguintes questões estão claras:
- Qual a importância a importância dessa descoberta para o desenvolvimento da ciência e da física moderna?
- Quais são as principais forças envolvidas no experimento? Se não houvesse ar na câmara, quais seriam as forças envolvidas?
- Qual a origem da carga elétrica das gotas?
- Como foi calculada a carga de um único elétron?
- É correto afirmar que a carga elétrica é quantizada?